Utilizados







































O mel é geralmente considerado um ambiente estéril devido à alta concentração de açúcares que dissecaria microrganismos, sendo assim foi testado 2 diluições de mel para avaliar o número de microrganismos por microlitro de mel. Em 0,1 μl de mel não foi possível identificar nenhum fungo ou bactéria nos meios de cultivo testados. Plaqueando o equivalente a 35 μl de mel por placa foi identificado um número variável de colônias, sendo que o mel produzido por abelhas nativas produziram um maior número de microrganismos associados.

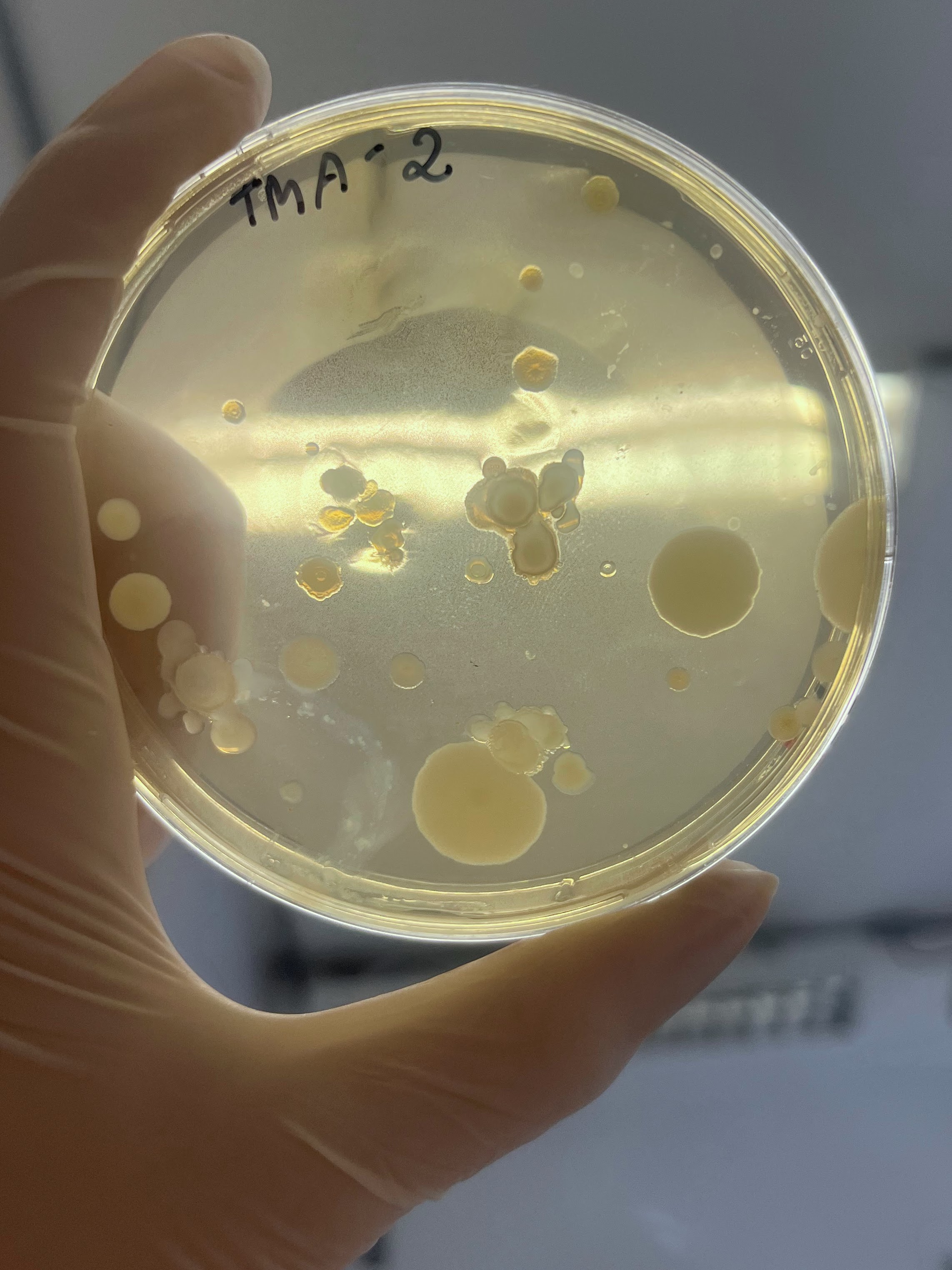
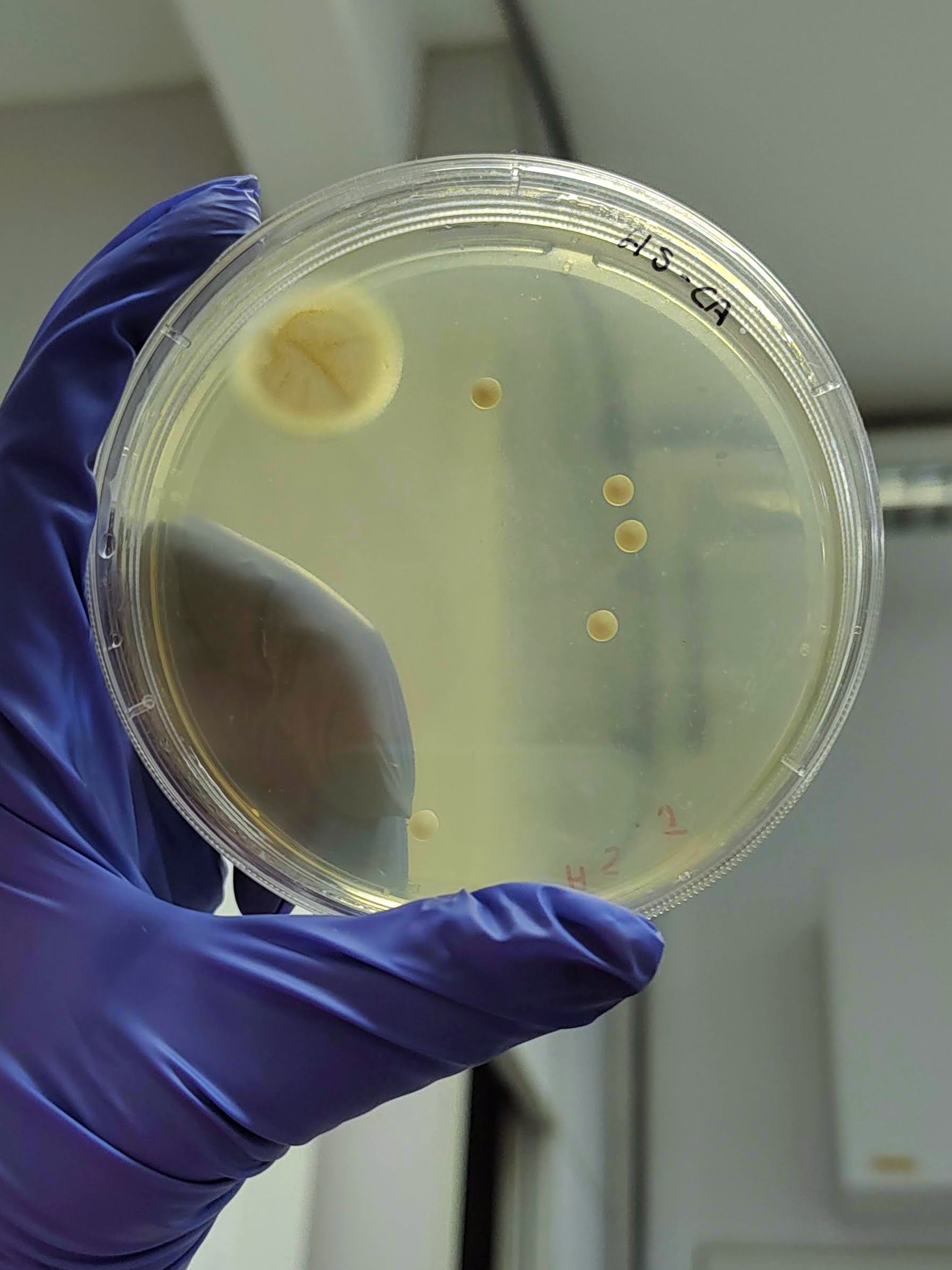
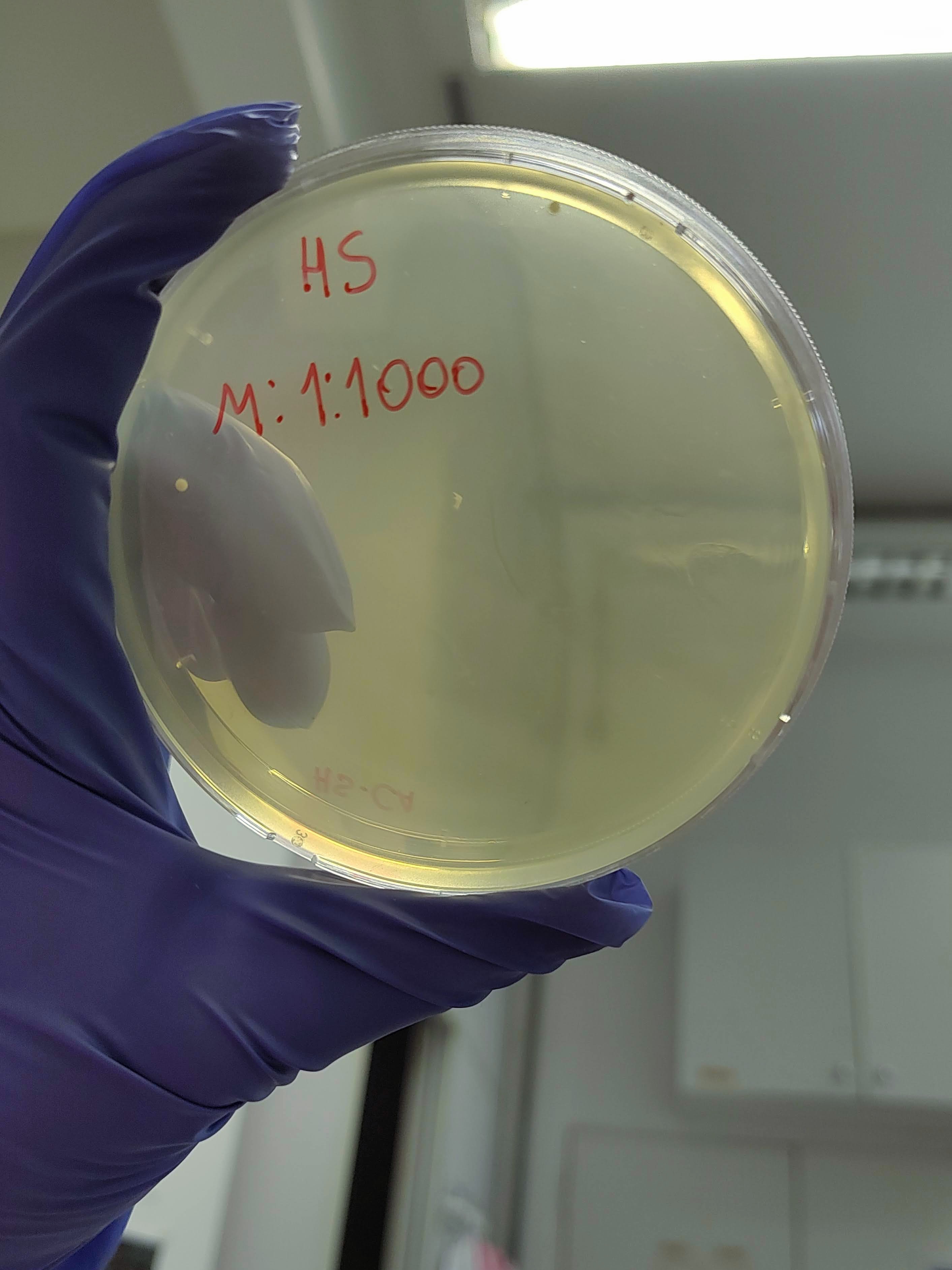
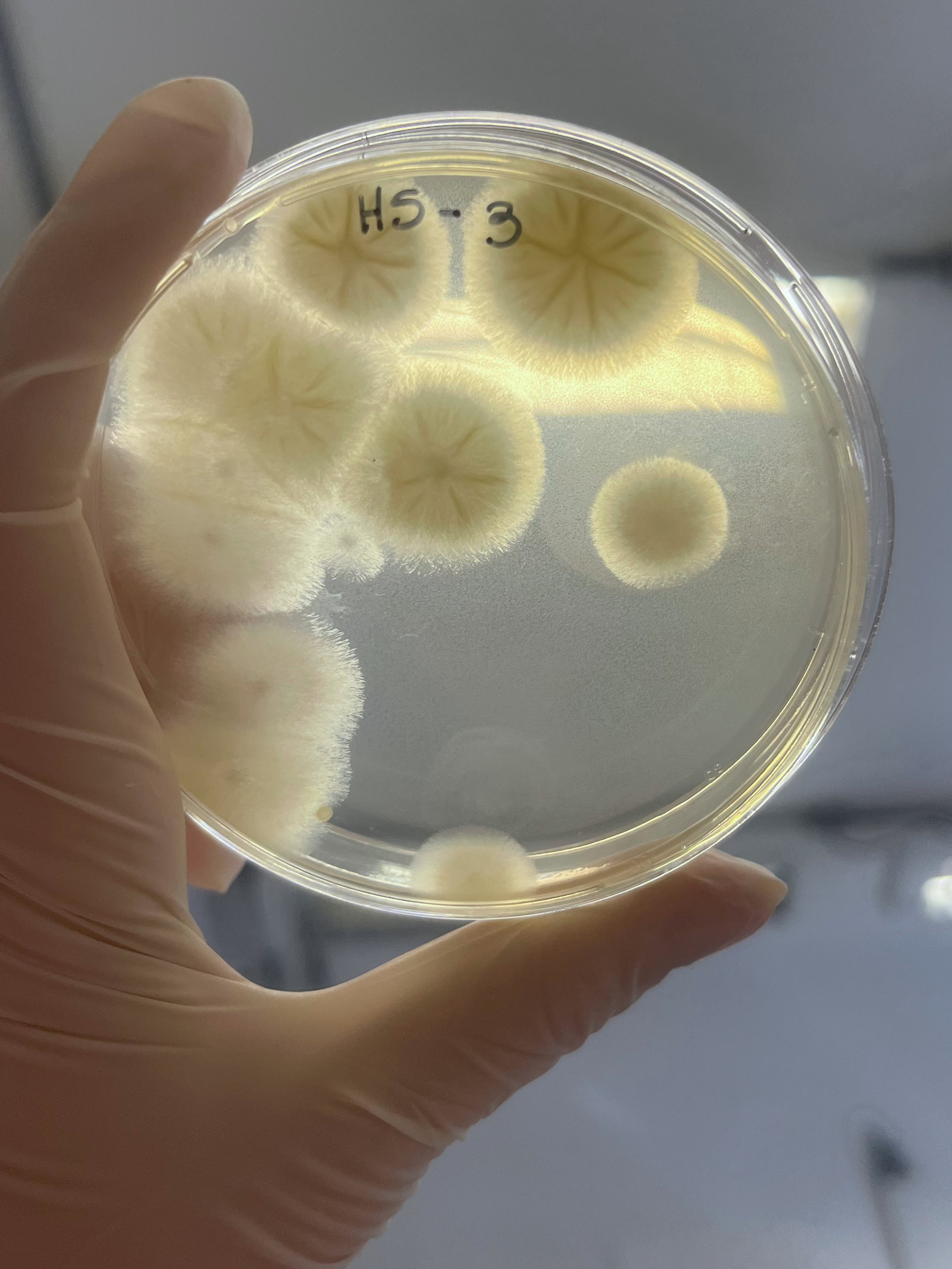
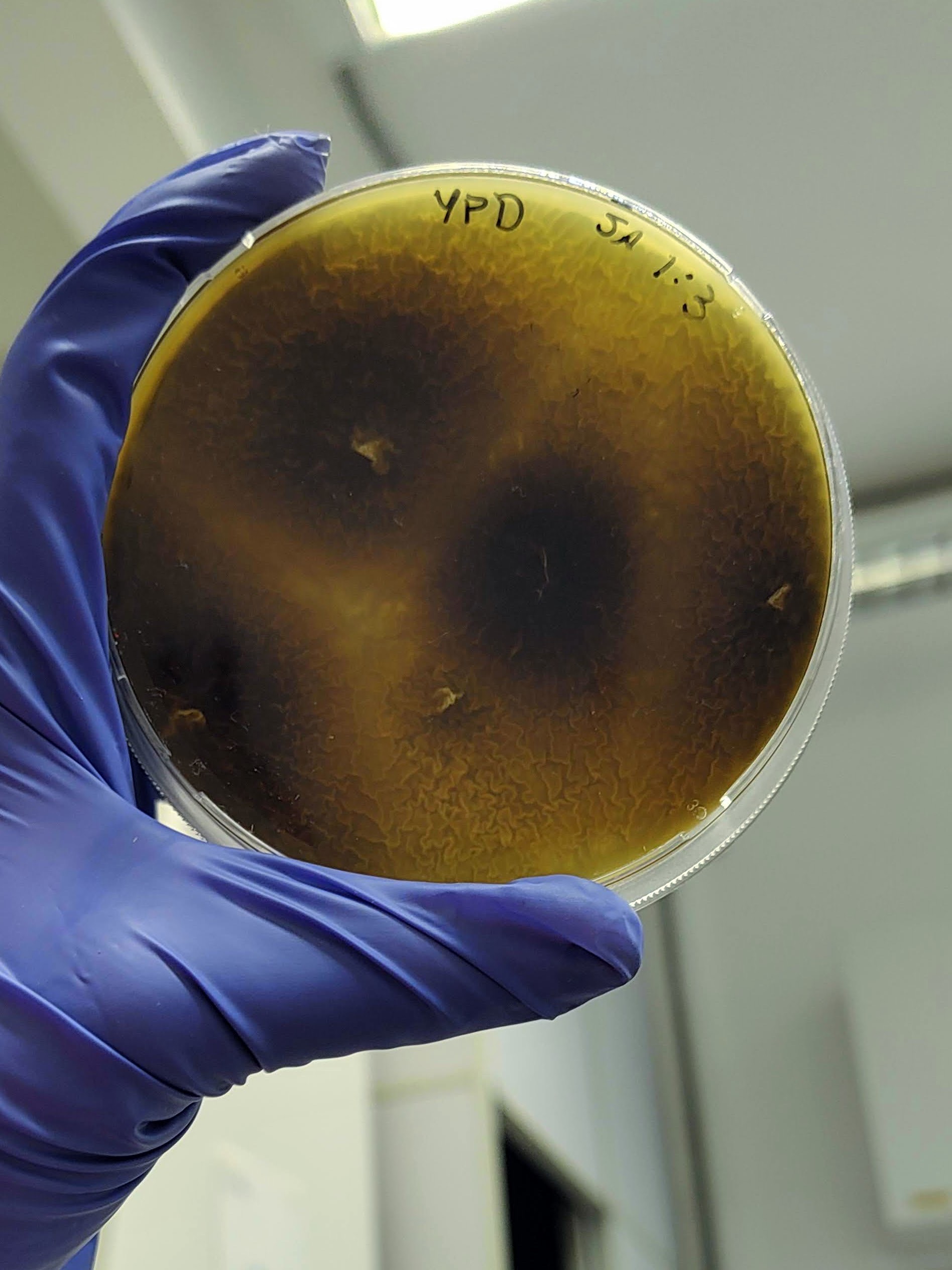
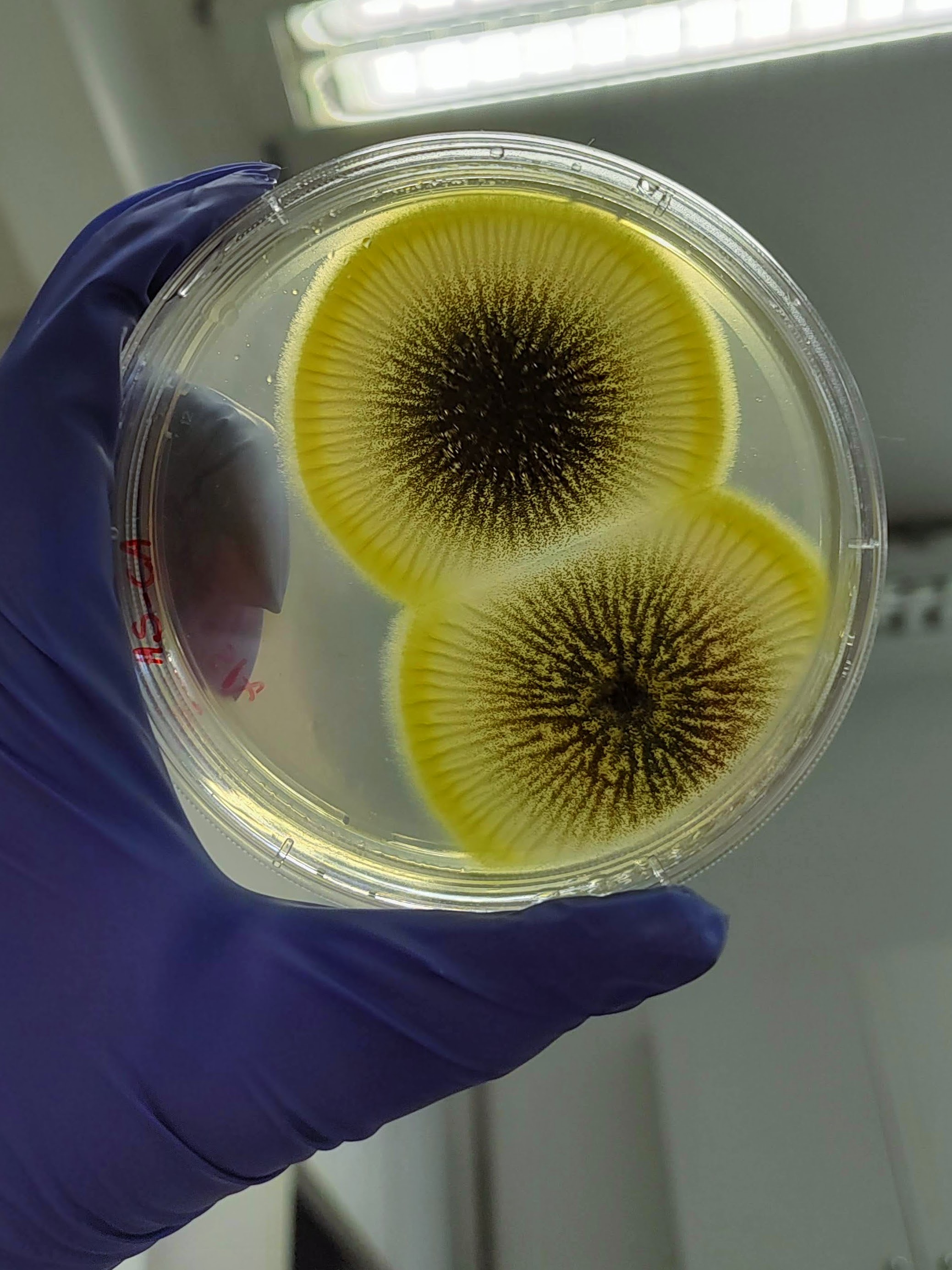
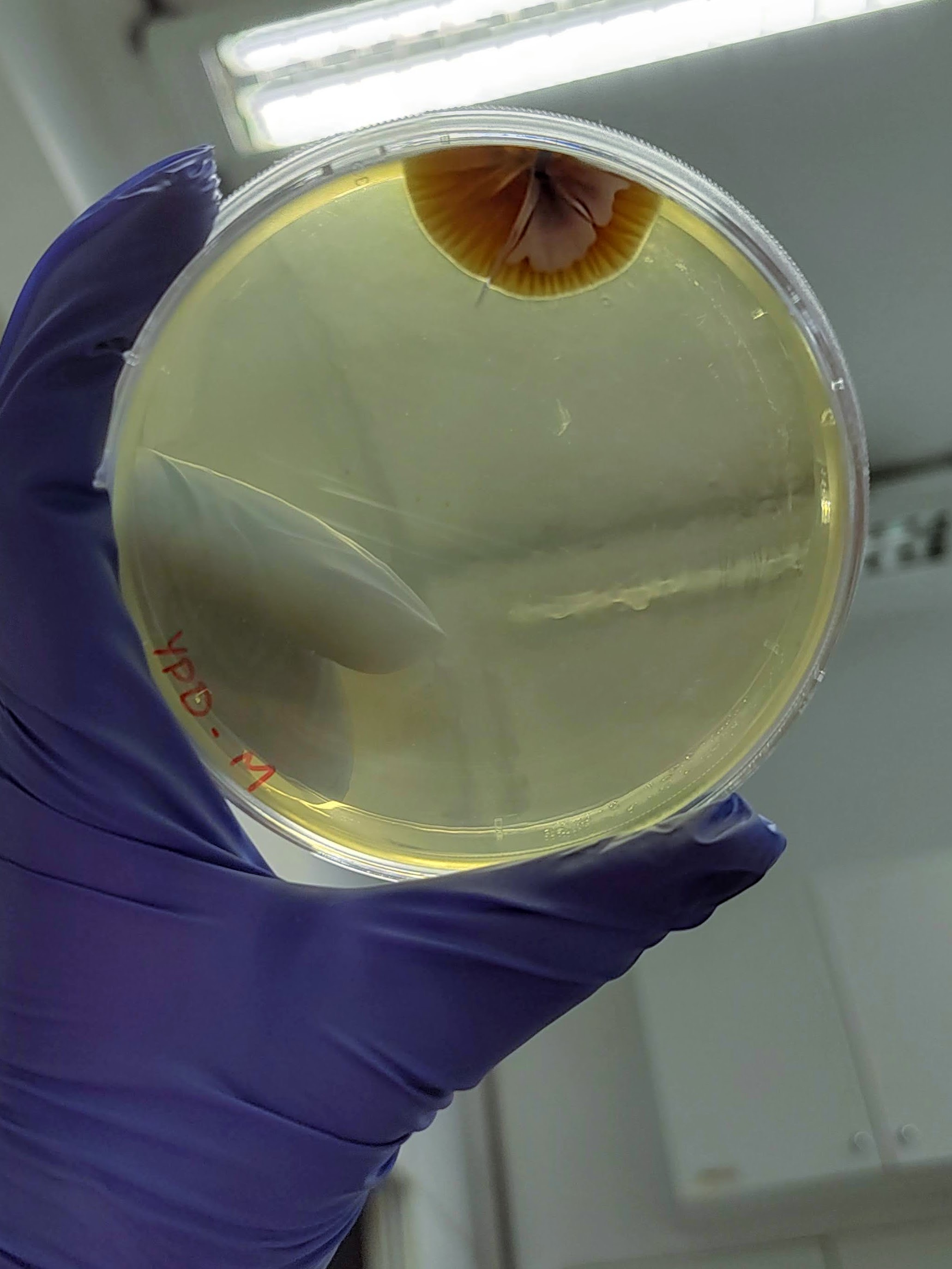
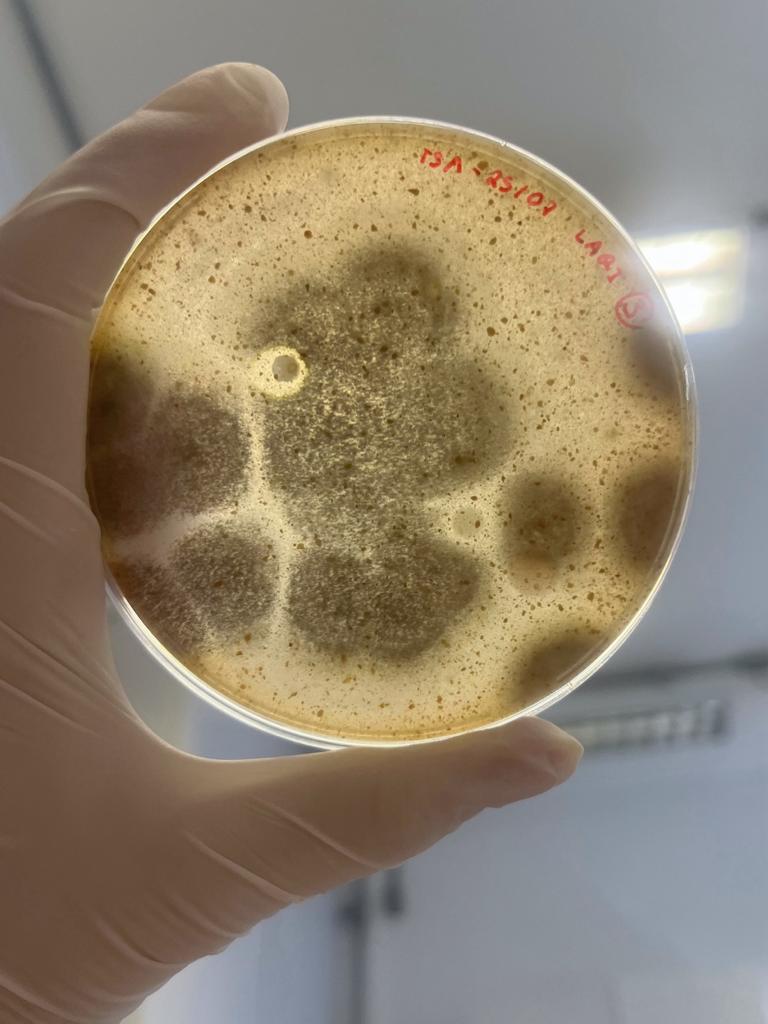
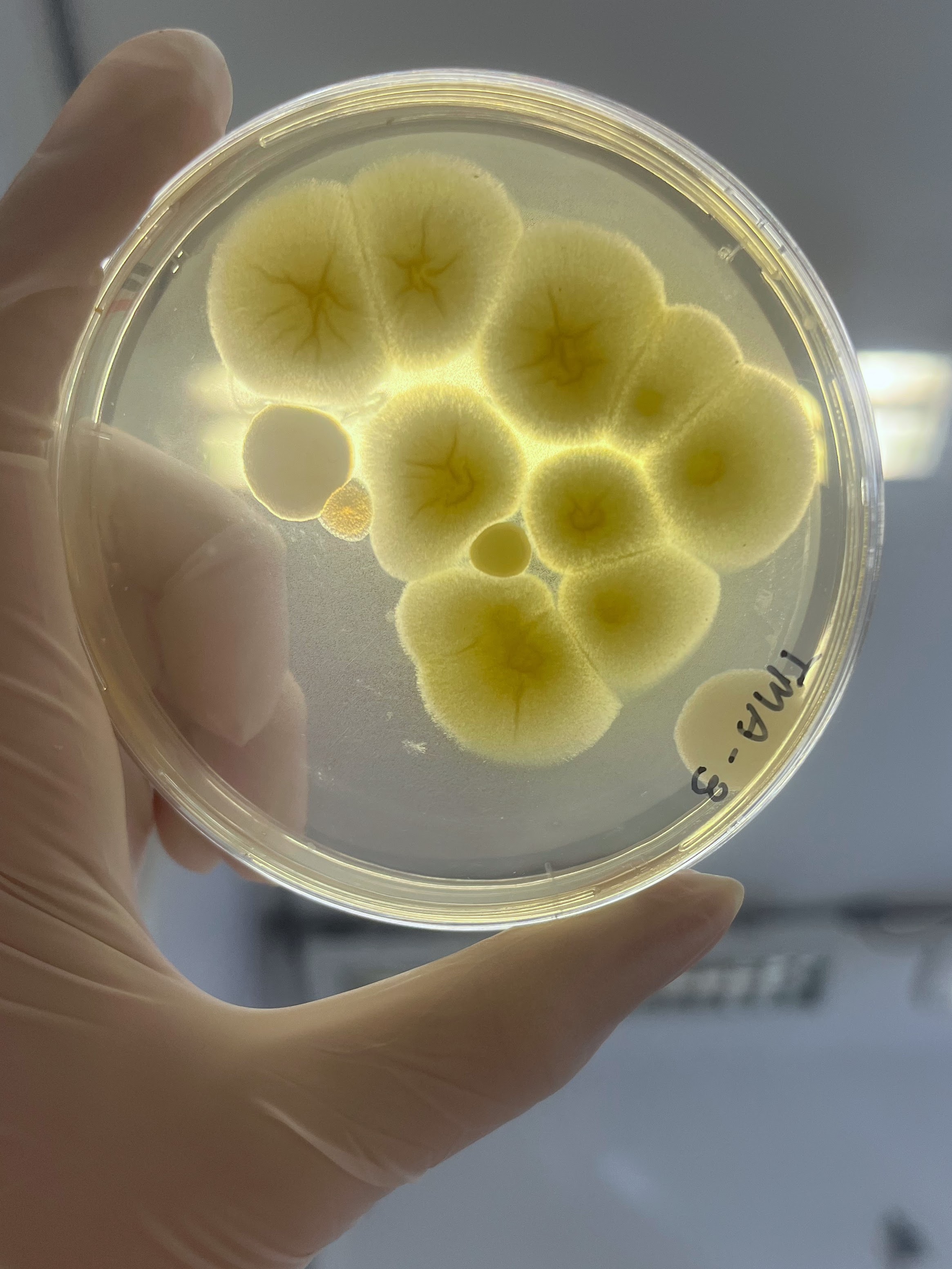
É interessante notar que a aparência das colônias formadas em placas variou significativamente dependendo da origem do mel, o que indica que os microrganismos foram realmente derivados do mel e não de contaminação laboratorial.
O gráfico abaixo illustra a quantidade de colônias cultivadas de cada mel e em cada meio de cultivo utilizado.
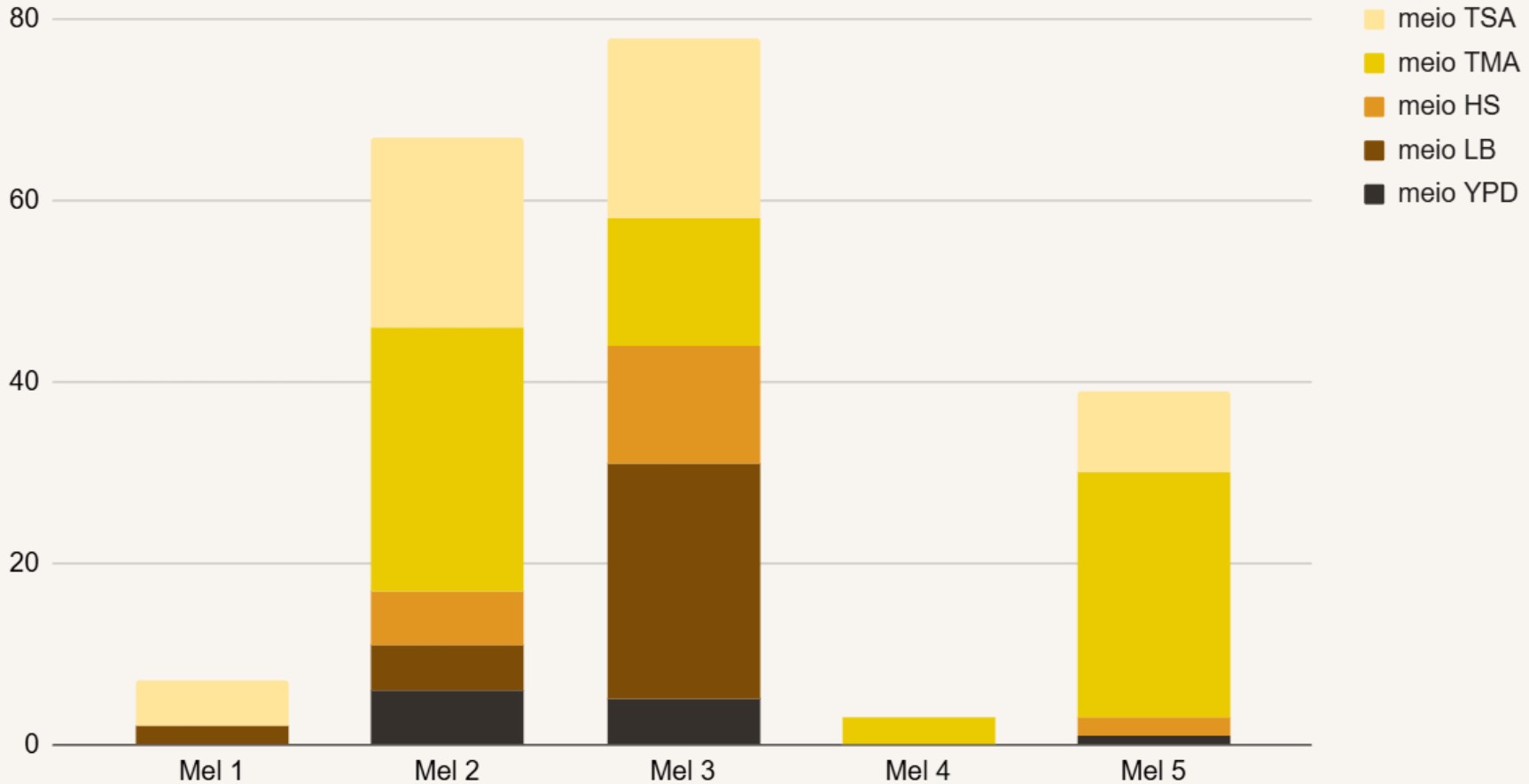
Para todos os microrganismos isolados, foi preparado estoques armazenados a -80°C, DNA genômico e realizados vários testes de halo, que indicam a capacidade de secreção de compostos com ação antibiótica e antifúngica.
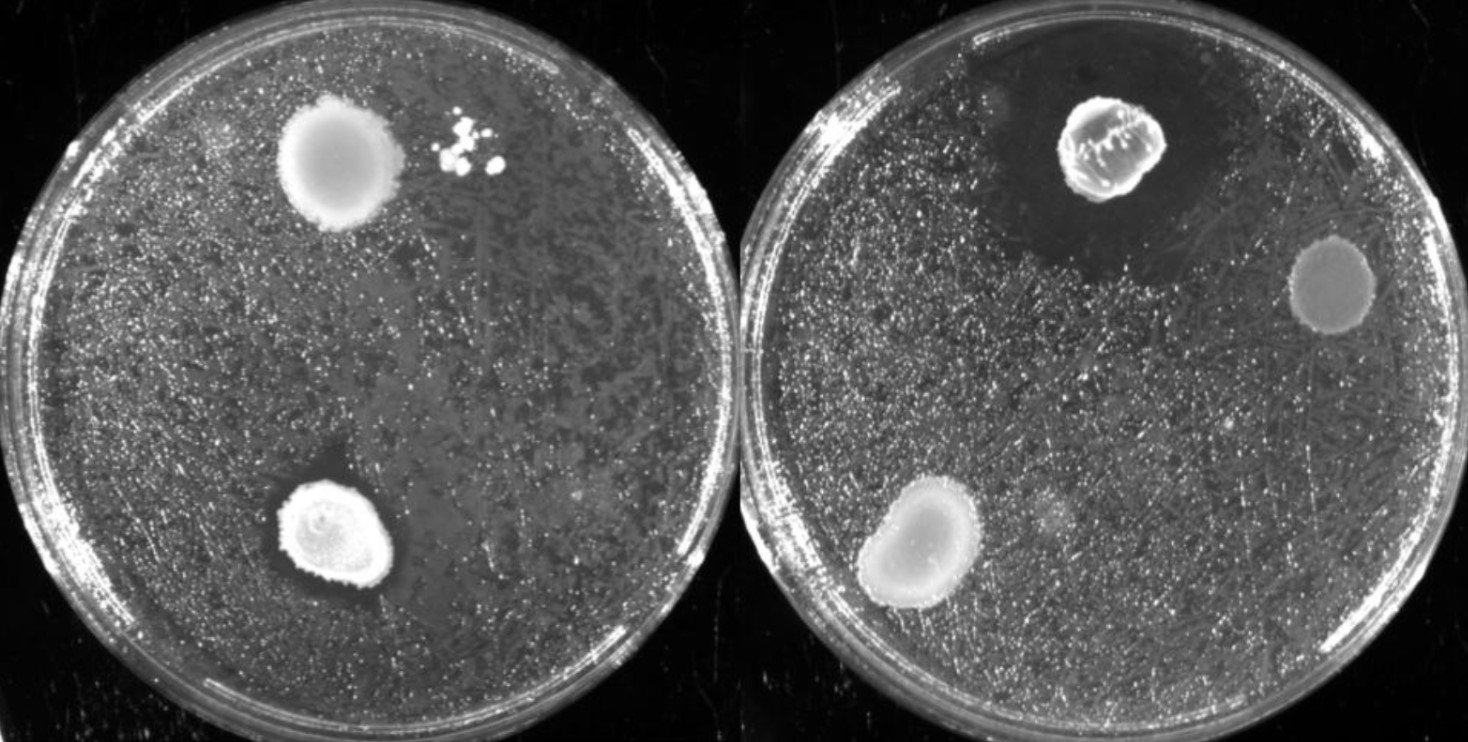
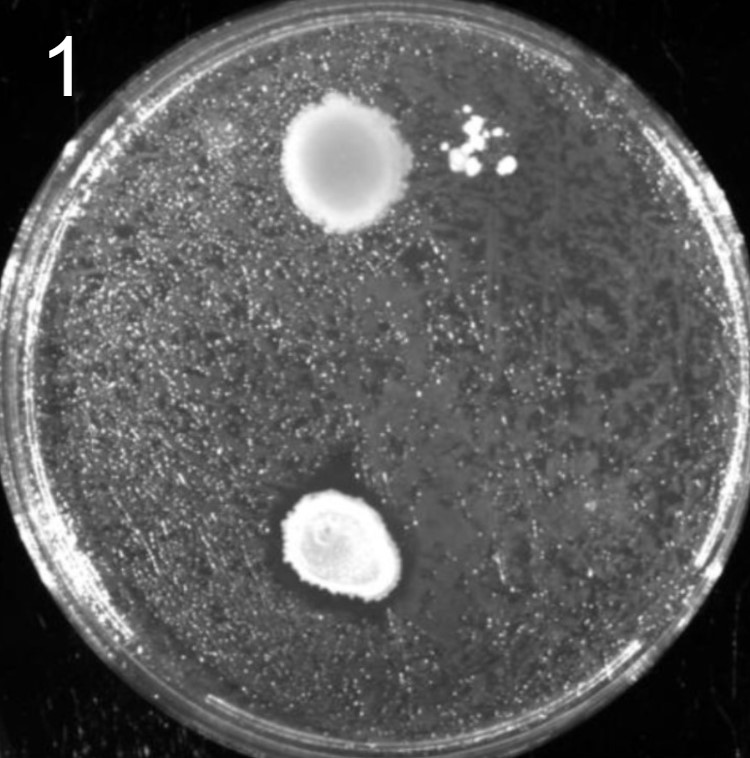
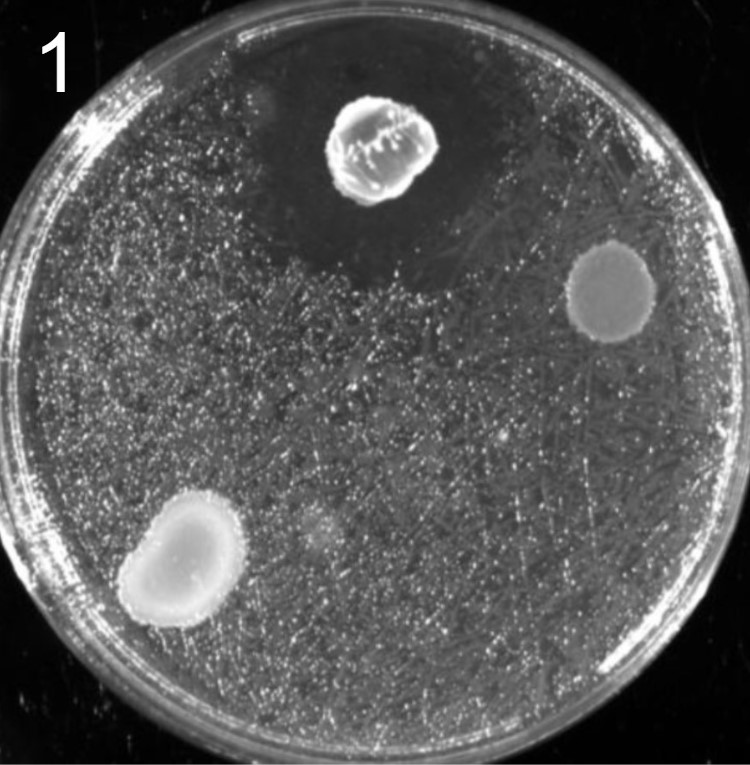
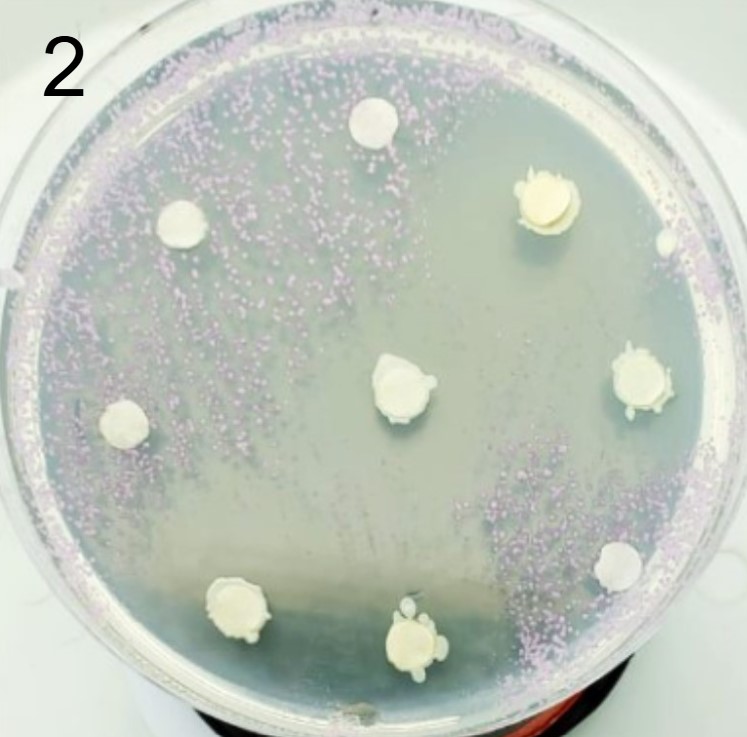
Esses testes de halo de inibição foram realizados contra 2 microrganismos padrão de laboratório: a bactéria E. coli(placas 1) e a levedura S. cereviseae(placas 2).
OBS.: As circunferências ao redor das colônias indicam uma região com inibição de crescimento do fungo ou levedura, demonstrando assim, a secreção de antimicrobianos.
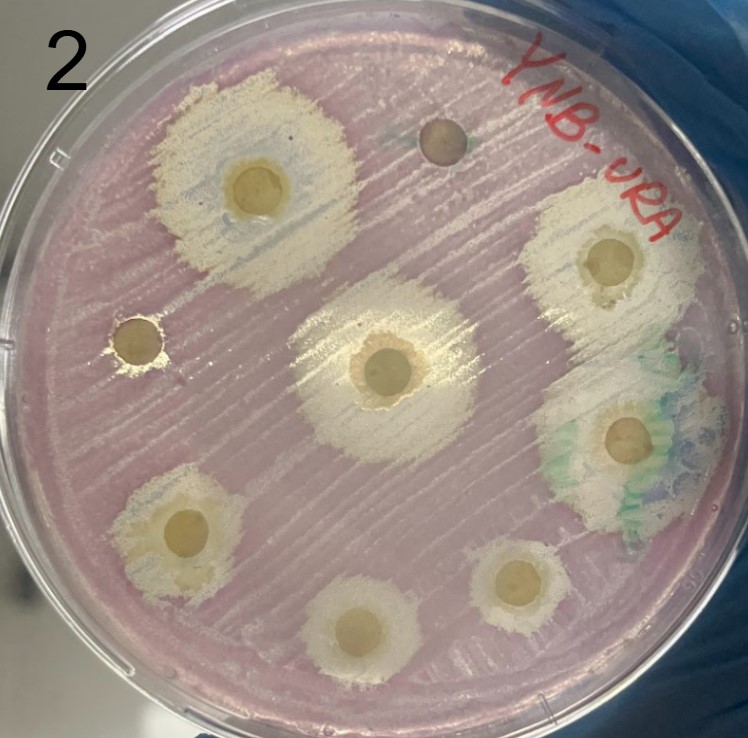
Além disso, foram realizados mais ensaios contra 7 micróbios prejudiciais na agricultura: a bactéria fitopatogênica X. Citri(placas 3), e os fungos Sclerotinia sclerotiorum(placas 4), Rhizoctonia solanum(placas 5), Fusarium oxysporum(placa 6), Rhizoctonia solani(placa 7), Botrytis cinerea(placa 8) e Fusarium verticillioides(placa 9).
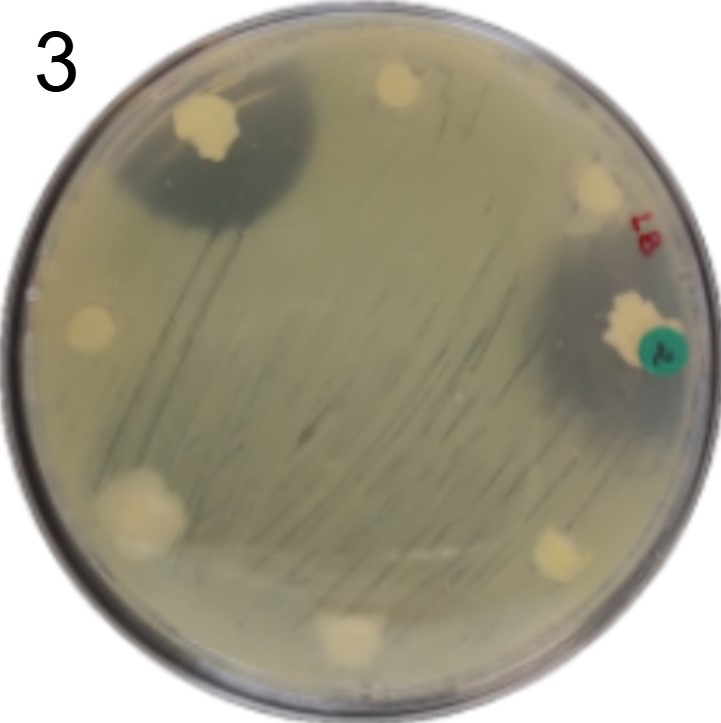
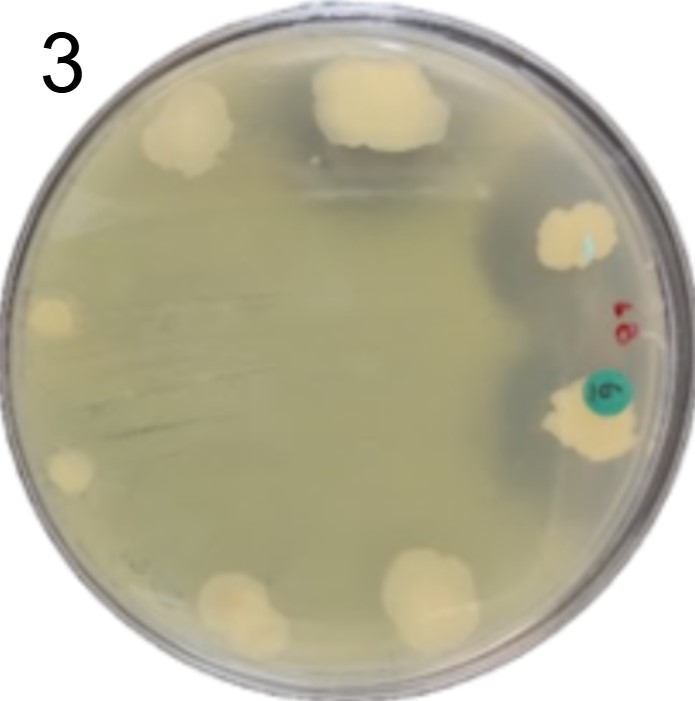
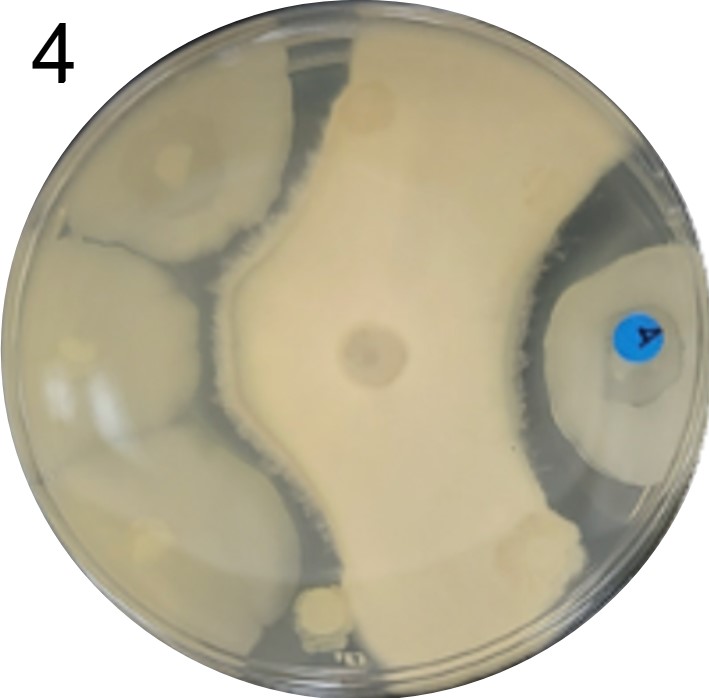
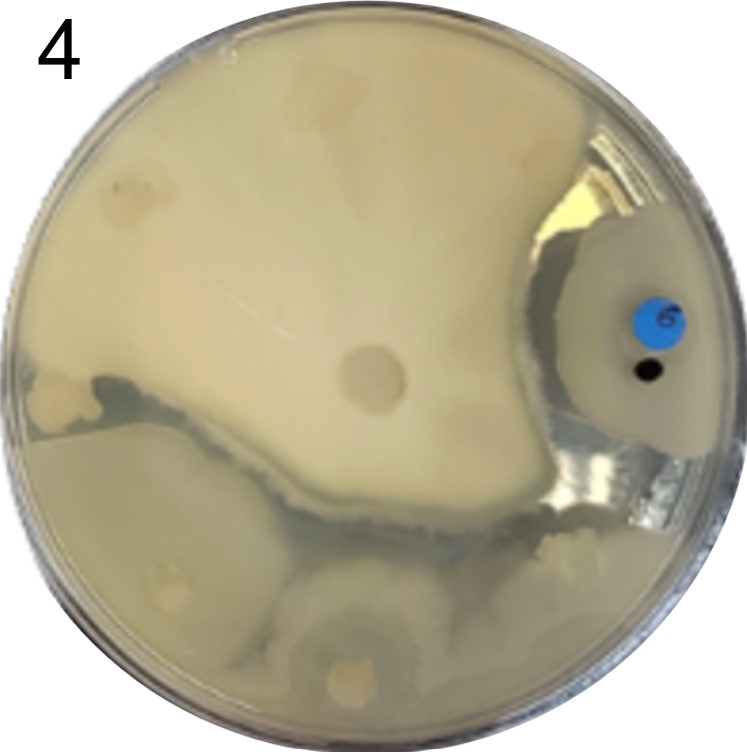
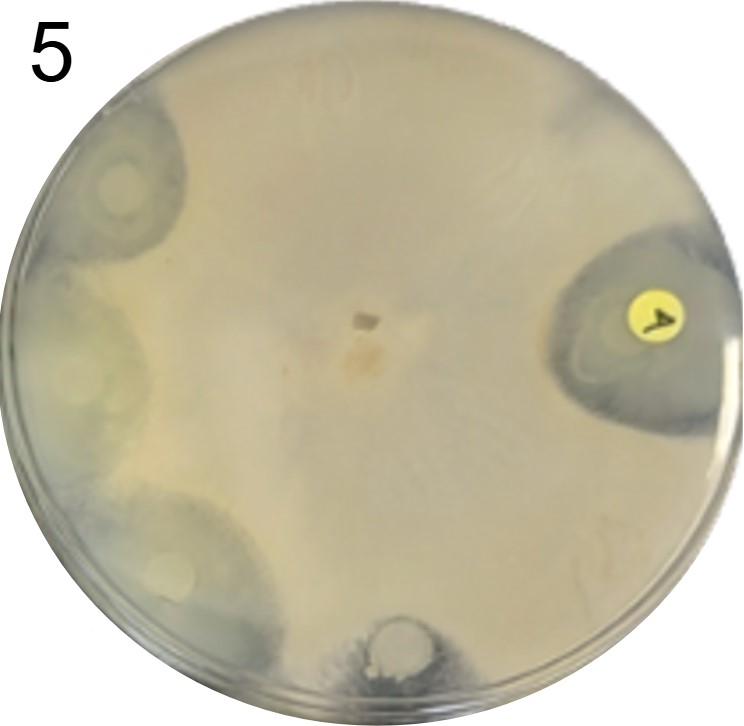
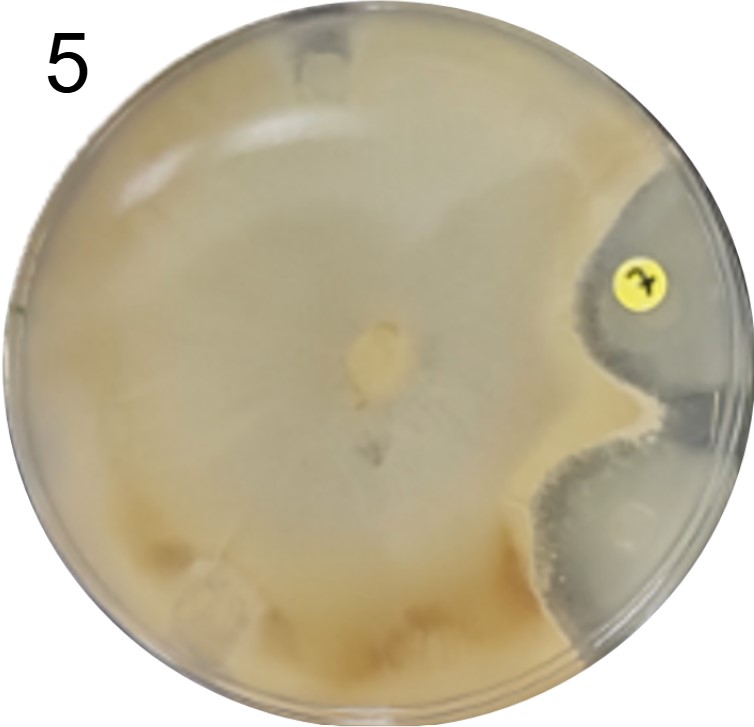
Incluímos nesse experimento para comparação, o controle biológico B. subtilis, vendida sob o nome comercial Serenade, identificado pelo adesivo colorido.
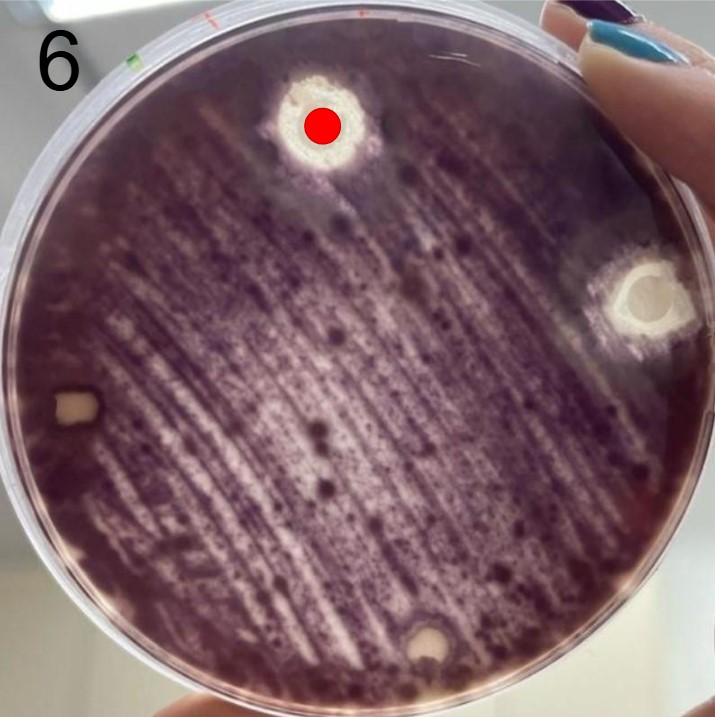
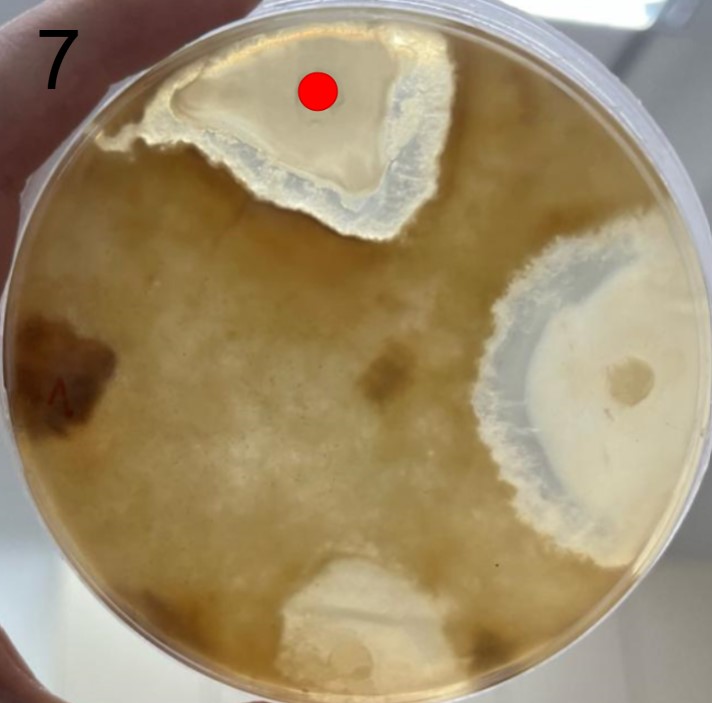
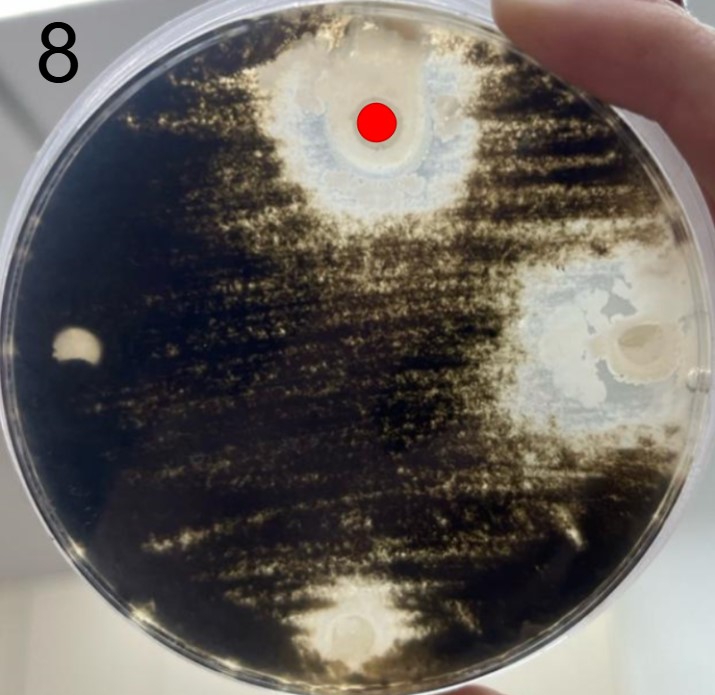
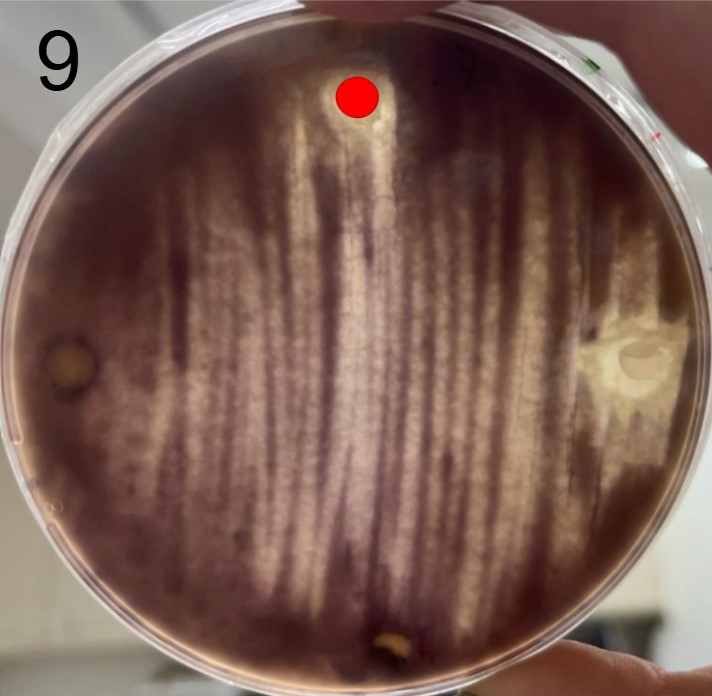
É possível observar que muitos dos nossos organismos produziram halos de inibição comparáveis ou até maior que o produto comercial. Além disso, as aparências diversas das colônias formadas pelos organismos capazes de secretar compostos e os tamanhos variados dos halos formados por eles indicam que o presente trabalho permitiu o isolamento de diversas espécies de organismos produtores de antibióticos e ou antifúngicos.
Foi realizada a genotipagem dos isolados que produziram antibióticos e/ou antifúngicos, visando identificar se os organismos são conhecidos ou se é trabalhado com novas espécies, potencialmente capazes de produzir novos antibióticos e antifúngicos. Foram otimizadas as reações de PCR para subsequente sequenciamento das regiões codificadoras para RNA ribossômico de fungos (18S) e bactérias (16S) e amplificadas diversas delas para envio para sequenciamento pelo método Sanger.
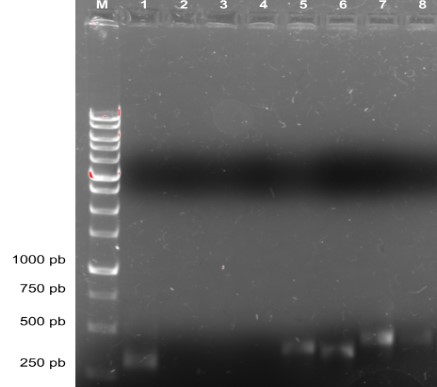
Os resultados de sequenciamento foram comparados com bancos de dados visando identificar as espécies com as quais trabalha-se. As sequências foram recebidas, analisadas utilizando o programa SnapGene Viewer e comparadas com um banco de dados online (BLAST) que contém as sequências de milhares de outros microrganismos.
Como resultado, foi descoberto que quase todos os microrganismos encontrados são de alguma espécie de Bacillus. Várias das sequências recebidas sugeriram espécies de microrganismos já descobertos que potencialmente produzem antibióticos e/ou antifúngicos.
Além disso, foi realizada a extração e purificação do DNA genômico utilizando beads magnéticos:

Foi realizado o sequenciamento por Nanoporo do microrganismo com maior atividade antimicrobiana em antibiogramas.
O sequenciamento do genoma foi realizado utilizando a tecnologia Nanoporo, MinION, que identifica as bases de DNA medindo alterações na condutividade elétrica, originadas das cadeias de DNA que passam pelos poros biológicos (LU et al., 2016)

Com isso, obteve-se os dados brutos. Porém, como a maioria dos reagentes usados neste trabalho estavam vencidos, a eficácia do sequenciamento do nosso genoma foi baixa, então será preciso fazer o sequenciamento mais vezes para que seja possível realizar a montagem.
E após isso, para que sejam identificados os genes responsáveis pela produção de antimicrobianos, iremos colocar o genoma pelo software AntiSMASH que irá fornecer todos os grupos de genes.
Mas enquanto não for possível realizar a montagem do nosso genoma, genomas da mesma espécie de bactéria que a nossa, já publicados, foram analisados utilizando a plataforma antiSMASH, para buscar grupos de genes ou agrupamentos de genes biossintéticos (BGC) que possam ser responsáveis pela produção de metabólitos secundários ou especializados, os quais podem ter ação antibiótica e/ou antifúngica.
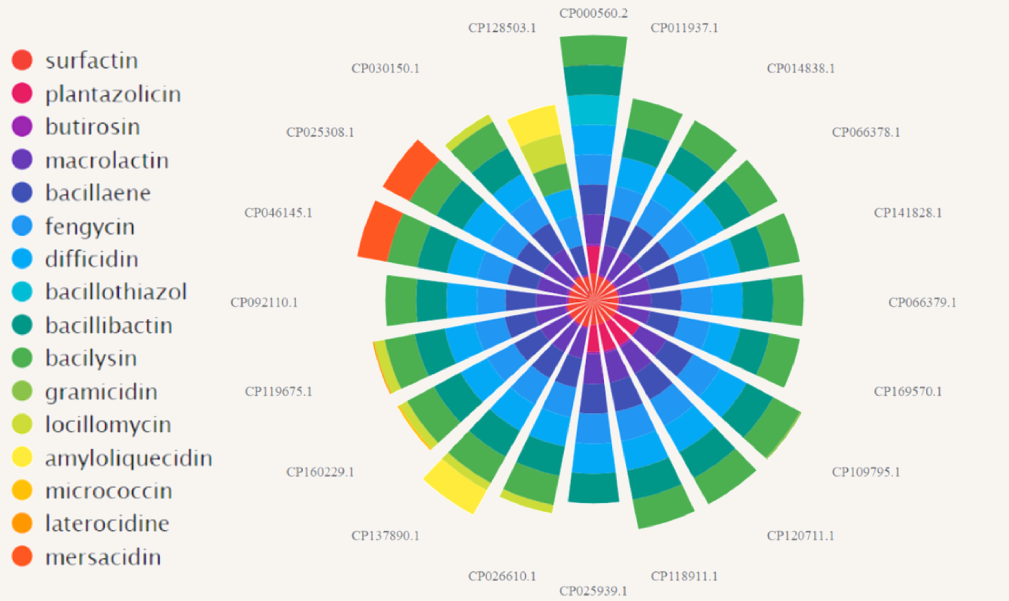
Esse gráfico mostra a diversidade dos genes responsáveis pela produção de antimicrobianos em linhagens da mesma espécie.
Para que outros também possam fazer a busca por BCGs, criamos uma aba nesse site que contém um link para um repositório do GitHub contendo instruções da análise.
CONCLUSÕES
Desse modo, através desse projeto caracterizamos as atividades antimicrobianas de 70 linhagens de microrganismos isolados de méis comerciais e foi descoberto que vários dos nossos microrganismos conseguem produzir mais antimicrobianos do que um produto comercial.
O próximo passo será realizar mais sequenciamento para que seja possível a montagem do nosso genoma e o aumento da sua capacidade produtiva, para que consigamos utilizá-lo futuramente como uma alternativa mais sustentável e eficiente aos produtos tóxicos utilizados na agricultura.



